Электрохимическая очистка
1. Электролиз
1.1 Электрохимическое катодное восстановление шестивалентного хрома на пористых инертных электродах
Технология позволяет восстанавливать шестивалентный хром в сточных водах и растворах без использования реагентов-восстановителей (сернокислого железа, сульфита и бисульфита натрия).
Наша технология выгодно отличается и от электрокоагуляционной технологии восстановления хрома:
✓ отсутствует проблема пассивации анодов и необходимость переполюсовки;
✓ отсутствуют затраты электродного материала (железа);
✓ рабочая плотность тока в наших электролизерах на порядок ниже, чем в электрокоагуляторах;
✓ отсутствует проблема взрывоопасности;
✓ отсутствует заиливание и необходимость чистки электродов;
✓ отсутствует ограничение по исходной концентрации шестивалентного хрома;
✓ колебания исходной концентрации шестивалентного хрома не влияют на стабильность процесса восстановления его;
✓ качество восстановления не зависит от анионного состава воды.
Cr2O7 + 14H+ + 6e → 2Cr3+ + 7H2O
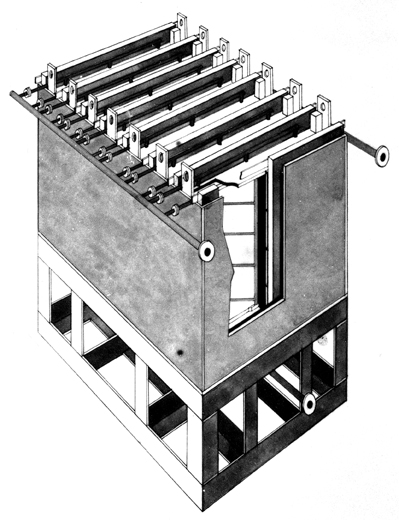
|
Электролизер с горизонтальным током |
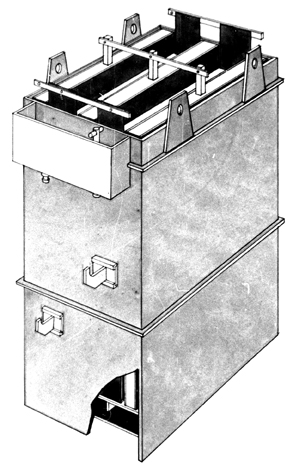
Электролизер с вертикальным током |
1.2 Технологии электрохимической деструкции трудноокисляемых веществ в сточных водах.
✓ технология электрохимического анодного окисления одноатомных и многоатомных фенолов
✓ технология электрохимического анодного окисления метанола
✓ технология электрохимического окисления трудноокисляемых органических веществ с участием пероксида водорода
✓ технология прямого электрохимического окисления ряда трудноокисляемых органических веществ с использованием высокопотенциальных анодов
✓ технология окисления трудноокисляемых органических веществ с помощью электрохимического варианта процесса Фентона
1.3 Технологии регенерации ряда отработанных технологических растворов и утилизации цветных металлов с использованием физико-химических методов
1.3.1 Технология регенерации безаммиачных сернокислых растворов (в том числе фенольных) кадмирования
В результате дебаланса анодного (растворение кадмиевого анода) и катодного (осаждение кадмия из раствора на поверхность деталей) концентрация кадмия в растворе растет от начальной (50 г/л) и при достижении 100 г/л раствор сбрасывается. Наша технология позволяет полностью регенерировать раствор с одновременным получением металлического кадмия. При локальном использовании электролизера регулирование состава рабочего раствора в гальванической ванне осуществляется непрерывно без остановки технологического процесса и без удаления раствора из ванны.

Электролизер с вращающимися катодами
для регенерации электролита кадмирования
1.3.2 Технология электрохимической регенерации отработанногораствора хлорного железа от травления меди
Регенерация производится в две стадии – осаждение металлической меди на катоде и последующее анодное окисление двухвалентного железа до трехвалентного. Процесс регенерации осуществляется по порционной схеме. Технология позволяет получать регенерированный раствор хлорного железа со следующими показателями:
содержание меди, г/л, не более – 5,
содержание двухвалентного железа, г/л не более – 10.

Электрохимическая установка для регенерации
отработанного раствора хлорного железа от травления меди
1.4 Технология обезвреживания сточных вод, загрязненных соединениями фтора, методами электрокоагуляции и гальванокоагуляции
Фтор в сточных водах обычно находится в виде фтористоводородной (HF) и кремнефтористоводородной (H2SiF6) кислот и их солей.
Традиционная очистка фторсодержащих вод производится в две ступени. В первой ступени обработка производится 5–10% раствором Ca(OH)2 в течение 10–15 минут до рН 10,5–11 с последующим отстаиванием в течение 1 часа. При этом образуется и выпадает в осадок CaF2. Произведение растворимости CaF2=4×10-11, растворимость его в воде при 293○К равна 16 мг/л, поэтому концентрация фторидов в воде после первой ступени обработки составляет 16–22 мг/л.
Для дальнейшего понижения концентрации фторидов во второй ступени при реагентной обработке используются трикальцийфосфат – Ca3(PO4)2, сернокислый алюминий – Al2(SO4)3 или активированная кремнекислота – смесь жидкого стекла и сернокислого алюминия. Очистка с использованием сернокислого алюминия и активированной кремнекислоты основана на сорбции ионов фтора на свежеосаждeнной гидроокиси алюминия.
Вторая ступень очистки более эффективно протекает при использованииметода электрокоагуляции с алюминиевыми электродами вследствие образования при растворении алюминиевых анодов более активной гидроокиси алюминия, чем при растворении реагента. Удельный расход алюминия при этом составляет 10–14 г/г на 1 г удаляемого фтора. Для частичного устранения пассивации анодов и снижения энергозатрат необходимо содержание в воде хлоридов не менее 100 мг/л. При рН стока менее 4 необходимо добавлять в случае отсутствия хлоридов NaCl, при рН более 6 – соляную кислоту до достижения оптимальной величины рН.
Концентрация фтора при оптимальных параметрах процесса снижается до 1–1,5 мг/л. Энергозатраты при этом составляют ~0,2 кВт·ч на 1 г. удаляемого фтора. После электрокоагуляционной обработки требуется отстаивание в течение 1 часа.
При небольших расходах сточных вод и невысоких концентрациях фторидов можно производить обработку в одну ступень электрокоагуляцией.
Можно также производить обработку фторсодержащих промывных вод методом гальванокоагуляции с загрузкой алюминиевого и медного скрапа в определeнных оптимальных соотношениях.
Для уточнения всех параметров и нюансов организации процессов обработки обращайтесь к нам.